Cétoines : les fées vertes du compost
Cetoniinae
Chaque fois que je vide les composteurs de mon jardin pour étaler le compost mûr, je récolte une bonne moisson de ces gros vers blancs dodus, parfois par dizaines : des larves de cétoines dorées ; je les mets de côté le temps de la vidange et je les remets dans le nouveau tas de compost en formation. Au fil des années, leur nombre ne cesse d’augmenter tout comme les splendides adultes auxquels ils donnent naissance : de gros scarabées massifs aux teintes vert à brun métallique si particulières et chatoyantes au soleil. Elles ont fait l’objet de nombreuses études scientifiques approfondies dans différentes directions avec plein de découvertes surprises : un excellent terreau pour une chronique zoom-nature !
Diversité
Dès lors qu’on parle de Coléoptères comme pour les cétoines, il faut s’attendre à un déluge de biodiversité ; bien que ne formant qu’une sous-famille des Scarabéidés, les Cétoniidés regroupent quand même 510 genres et plus de 4000 espèces dans le monde. En France, outre les trichies (Trichius), la cétoine punaise (Valgus hemipterus), les draps mortuaires (Oxytherea), les cétoines velues (Tropinota), cette sous-famille regroupe les « vraies » cétoines aux teintes métalliques vertes à noires avec au moins 14 espèces réparties dans deux genres proches d’aspect : Cetonia et Protaetia. Comme en plus certaines de ces espèces sont très variables, l’identification devient vite compliquée si l’on veut être rigoureux ! Dans cette chronique nous ne parlerons que des deux espèces que l’on rencontre assez facilement dans les jardins (et encore cela dépend des régions !) : la cétoine dorée (Cetonia aurata) extrêmement commune et la cétoine cuivrée (Proteatia cuprea), nettement moins commune mais régulière, en mélange avec la précédente.
Sans vouloir devenir un expert es-cétoines, on peut les distinguer (1) néanmoins en les capturant à la main ce qui est relativement facile vu la lourdeur de ces gros scarabées et en les examinant de près. Sur le dessous d’une rouge cuivreux, à la jonction entre l’abdomen et le thorax, on note une pièce allongée, une saillie du thorax, qui est soit globuleuse (comme une boule d’attelage de voiture) pour le genre Cetonia, soit aplatie pour le genre Protoetia. De dessus, on prêtera attention à la coloration générale même si celle-ci varie énormément : vert doré métallisé à nettement violacé avec des petites taches transversales blanches assez nombreuses sur les élytres (les ailes très dures du dos) pour la cétoine dorée ; vert foncé à bronze avec peu de taches blanches (voire pas du tout) pour la cétoine cuivrée. Ajoutons un critère pour cette dernière à observer de très près : au niveau des genoux des pattes pliées, on note une petite tache claire faite d’écailles blanches serrées, le petit détail des spécialistes mais qui se voit même sur les photos de cétoines prises de près !

Cétoine cuivrée : on devine les genoux blancs 
Cétoine cuivrée à gauche et dorée à droite 
Saillie sternale ronde d’une cétoine dorée ; noter le dessous cuivreux 
Saillie sternale aplatie de cétoine cuivrée 
Plaque d’écailles qui donne cet aspect blanchâtre aux genoux de la cétoine cuivrée
Spécialisées
Une première génération d’adultes apparaît dès début avril, avec un pic en mai-juin, jusqu’en juillet ; les années chaudes (de plus en plus souvent !), quelques adultes émergent en septembre-octobre sans se reproduire : ils hibernent et s’accoupleront au printemps suivant. Les cétoines dorées fréquentent divers milieux avec une dominante de buissons fleuris : lisières et clairières, friches, haies bocagères et, de plus en plus, les jardins fleuris des villes et villages (voir le paragraphe sur les larves). Elles recherchent les floraisons de grandes herbacées telles que les chardons et cirses, diverses ombellifères (comme les berces), les iris, … et surtout celles de buissons et d’arbres : sureaux noirs, aubépines, églantiers, cornouillers, troènes, … et, dans les jardins, les lilas, les pyracanthas, les spirées et surtout les roses. Les anglais les surnomment « rose chafer », les hannetons des roses. Le verbe to chafe signifie irriter, grignoter et traduit bien la manière dont se nourrissent les cétoines dorées : la tête plongée au cœur de la fleur, au plus près des étamines et du pistil, elles « fourragent » méthodiquement, consommant pollen et nectar avec avidité. La génération automnale, plus rare (voir ci-dessus) recherche plutôt les fruits en maturation à une période où, il est vrai, les fleurs sont devenues plus que rares !

Cétoine dorée sur une viorne ornementale 
Cétoine à moitié cachée dans une rose 
Rassemblement de cétoines dorées sur la floraison du pyracantha
Une étude au microscope électronique (2) des pièces buccales a permis de découvrir chez les cétoines un dispositif original pour la récolte du pollen. Un petit rappel pour s’y retrouver : quand on regarde la tête de face, en partant de l’extérieur, on trouve la paire d’antennes terminée par une massue de 3 articles, puis les mandibules, ensuite les mâchoires ou maxillas et enfin une pièce unique centrale, le labre ou labium avec la bouche. Les mandibules, dotées chacune d’un petit palpe, portent vers l’intérieur une pièce avec de longues soies (galea) qui sont couvertes d’un liquide les rendant humides ; en pivotant vers l’intérieur lors des mouvements, cette brosse humide récolte le pollen qui s’y colle. Les grains de pollen, repris par une brosse courte plus interne, migrent vers l’intérieur en direction des mandibules où ils sont mastiqués : l’analyse du contenu du tube digestif montre la présence de grains éclatés et d’autres avalés intacts. D’ailleurs, quand on regarde les pièces buccales, on est frappés par les mandibules réduites qui n’ont pas du tout l’apparence de pinces fortes comme nombre de coléoptères (voir l’exemple du lucane). Chez d’autres coléoptères floricoles, on trouve d’autres dispositifs de collecte qui sont apparus indépendamment et impliquent des structures différentes.

Sous la tête : les soies raides servant à la collecte du pollen 
Détail d l’ensemble mandibule/mâchoire avec les brosses à pollen 
Labre poilu qui cache l’ouverture de la »bouche » 
Cétoine dorée barbouillée de pollen (sur une ombellifère)
Renifleuses
Dans certains pays de l’Est comme en Hongrie ou en Croatie, les cétoines dorées sont considérées comme des ravageurs dans les plantations de pêchers ; on les accuse d’abîmer les fleurs qui ne peuvent ensuite être fécondées et d’attaquer en fin d’été les jeunes fruits en maturation et de causer ainsi des dégâts qualifiés d’importants. On a donc beaucoup étudié des moyens de lutte et de suivi de ces populations en mettant au point des pièges attractifs odorants comme il en existe pour nombre d’insectes. On savait que d ‘une manière générale les cétoines réagissent à un large spectre de composés odorants émis par les fleurs nourricières. Après expérimentation, un mélange de trois composés volatiles odorants, parmi les plus communs chez de nombreuses fleurs, a été lis au point et s’avère efficace : le 3- méthyl eugénol, le 1-phényléthanol and le (E)-anethol dans des proportions identiques. L’addition de lavandulol augmenterait le pouvoir attractif. Le problème de ces pièges est qu’ils capturent d’autres insectes dont les abeilles pollinisatrices ! En testant ces pièges, on s’est rendu compte que la couleur de ce dernier avait un impact : la couleur bleu clair semble la plus attractive vis-à-vis des cétoines dorées et cuivrées. Rappelons que les couleurs réfléchies par les fleurs ou perçues par les insectes ne correspondent pas forcément à celles que nous percevons avec nos yeux d’humains ce qui explique que souvent les cétoines fréquentent en fait des fleurs blanches ou rose !
Bourdonnantes
Si les cétoines sont assez lourdaudes dans leurs déplacements sur les fleurs et les inflorescences, elles sont capables de décoller en un éclair dès qu’elles se sentent en danger. Le décollage se fait brusquement dans un fort bourdonnement qui fait toujours un peu sursauter. La majorité de coléoptères écartent leurs élytres à 180° ou presque pour déployer en même temps la seconde paire d’ailes membraneuses qui effectue les mouvements permettant le vol. Les cétoines se démarquent complètement de ce schéma : on a l’impression que leurs élytres ne bougent pas du tout et elles déploient leurs ailes membraneuses via une sorte d’échancrure bien visible de profil à l’avant des élytres. En effectuant les recherches pour rédiger cette chronique, sur au moins trois sites internet, nous avons trouvé mention du fait que les élytres étaient soudées et donc forcément incapables de se déployer. Or, cette information est fausse et sans doute liée à une mauvaise interprétation de ce que l’on voit à l’œil nu. Une étude en microcinématographie (4) montre clairement que les élytres se soulèvent très légèrement, imperceptiblement et selon un axe de rotation particulier et très limité. Ce dispositif autorise ainsi sans doute une plus grande rapidité du déploiement des ailes postérieures. Une fois en l’air, les cétoines filent bon train et disposent de ce fait d’une bonne capacité de dispersion dans leur environnement ; cela leur permet aussi de se déplacer au fil des floraisons qui défilent au cours du printemps.

Sur une cétoine morte, un élytre a été enlevé : on voit l’aile membraneuse repliée en dessous 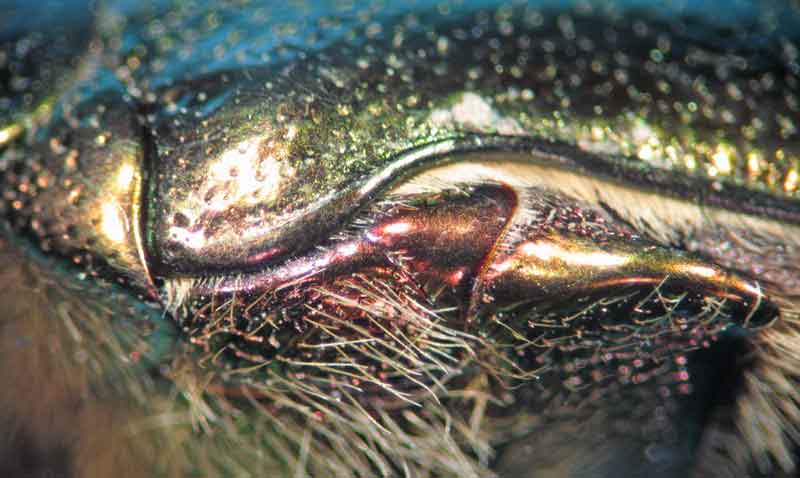
Echancrure latérale par où sort l’aile membraneuse 
Aile membraneuse dépliée ; noter l’articulation médiane qui permet la pliure au repos 
Pattes griffues et épineuses
Parfois, en cas de menace, les cétoines peuvent aussi adopter le comportement de « faire le mort » (thanatose) que l’on retrouve chez nombre de coléoptères (voir l’exemple du crache-sang).
Vers blancs
Les accouplements, souvent répétés et laborieux, se déroulent en fin de printemps à l’occasion des rassemblements sur les arbustes fleuris. Les femelles pondent en mai juin des œufs blanchâtres en forme de petites billes qui éclosent assez rapidement pour donner des larves dites mélolonthoïdes (de Melolontha, le nom latin du hanneton), très connues sous l’appellation populaire de vers blancs, nom incorrect car elles possèdent bien des pattes ! On les reconnaît à leur tête durcie et brunâtre, dotée cette fois de mandibules bien développées, et à leur corps dodu courbé s’élargissant au bout de l’abdomen : à la dernière mue, elles atteignent presque 4 à 5cm de long.

Larve de cétoine : noter le bout de l’abdomen très renflé 
Détail des mandibules très développées contrairement aux adultes 
Ce n’est pas un « ver » : elle a 3 paires de pattes ! 
Extrémité de l’abdomen
Ces larves ressemblent physiquement à celles des hannetons (qui sont nettement jaunâtres avec une grosse tête et des pattes plus longues) mais ne se nourrissent pas du tout de la même manière : celles des hannetons creusent des galeries dans le sol pour ronger les racines des plantes (d’où leurs mandibules très développées) alors que celles des cétoines se nourrissent de matériaux en décomposition.
Quand la larve a atteint sa taille maximale, elle se confectionne une sorte de coque faite de particules de terre agglomérées dans laquelle elle se nymphose. Une lectrice assidue, S. Carpentier, m’a communiqué une photo de ces « cocons » de terre trouvés dans son compost.

Originellement, les cétoines dorées et cuivrées semblent avoir été confinées au bois vermoulu en décomposition (tronc creux, souches, branches mortes, …) et faisaient donc partie des insectes saproxyliques (voir l’exemple du lucane pour cette notion). Au cours des dernières décennies, sans doute suite à la disparition de leur habitat favori, elles ont opéré un changement radical en s’adaptant à un régime beaucoup plus généraliste de matières organiques en décomposition : copeaux de bois pourrissants utilisés comme paillage, tas de feuilles mortes ou de fumier, tas de compost ou terreau des pots de fleurs. Ceci explique leur abondance désormais en milieu péri-urbain avec la généralisation du compostage dans les jardins. Ce changement est très spectaculaire en Europe occidentale où il tend à se généraliser, aidé de plus par des campagnes d’information et la sensibilisation des jardiniers à des pratiques plus respectueuses de l’environnement. En Angleterre, on a initié une opération intitulée BB4B (Burry a bucket for Beetles) destinée aux lucanes cerf-volants (voir la chronique) et qui peut aussi profiter aux cétoines : on enterre un pot de fleurs percé de gros trous, rempli de copeaux de bois (non traité) avec 1/3 de terre et l’enterrer jusqu’au bord, laissant juste dépasser le rebord.

Améliorantes

Paillis de bois fragmenté 
Tas de compost dans un jardin 
Les composteurs entrent de plus en plus dna sue paysage ordinaire des jardins urbains
La faiblesse nutritive de cette alimentation explique que le cycle s’étale sur deux ans (5) : la première année, la jeune larve effectue deux mues puis hiberne ; l’année suivante, elle en refait deux autres et vers mi-juillet, elle se fabrique un cocon de terre et de fibres végétales collée de la taille d’un gros gland dans lequel elle se métamorphose en nymphe immobile. Dès mi septembre, l’adulte est formé mais, le plus souvent (voir ci-dessus), ne sort pas : il va hiberner et émerger dès le début avril de l’année suivante.
Une étude sur une espèce proche méditerranéenne (Cetonia aurataeformis), inféodée au bois mort, a exploré l’impact de leur alimentation sur le milieu. Les larves produisent une grosse quantité d’excréments qui persistent au moins un an et transforment ainsi le bois en un nouveau matériau de structure différente, très fractionnée ; l’analyse chimique de ces excréments montre qu’ils sont plus riches en azote et phosphore que le substrat originel, un tour de force surprenant. Les larves décomposent les sucres et la lignine du bois et on pense qu’elles seraient capables de fixer de l’azote (bactéries symbiotiques ??). Les larves de cétoines transforment le bois mort peu nutritif, compact en un « terreau » fin et enrichi qui va servir de substrat à de nombreuses larves d’autres insectes saproxyliques : ainsi, les cétoines seraient des espèces « parapluies ». Si on transpose ces résultats à nos cétoines dorées, on peut fortement supposer qu’elles font de même avec le compost et contribuent à en faire un terreau de haute qualité ! Raison supplémentaire donc pour conserver précautionneusement ces larves dans votre compost, souvent détruites car confondues avec des larves de hannetons ; soit dit en passant, vu la raréfaction de ces derniers, ils mériteraient tout autant d’être protégés quand on trouve en bêchant !
BIBLIOGRAPHIE
1) Une clé illustrée des Cetoniidae de France.Pierre ZAGATTI et Anne GUY. OPIE
2) Pollen grains adhere to the moist mouthparts in the flower visiting beetle Cetonia aurata (Scarabaeidae, Coleoptera). Florian Karolyi et al. Arthropod-Plant Interactions (2009) 3:1–8
3) New co-attractants synergizing attraction of Cetonia aurata aurata and Potosia cuprea to the known floral attractant. J. Vuts, Z. Imrei& M. To thJ. Appl. Entomol. 134 (2010) 9–15 a 2009
4) Geometry of elytra opening and closing in some beetles (Coleoptera, Polyphaga).Leonid Frantsevich et al. The Journal of Experimental Biology 208, 3145-3158 ; 2005
5) The Rose Chafer Cetonia aurataL. (Coleoptera: Scarabaeidae: Cetoniinae) in Essex: distribution and some aspects of its ecology.MARIA FREMLIN Essex Naturalist (New Series) 35 (2018)
6) Action of the saproxylic scarab larva Cetonia aurataeformis (Coleoptera: Scarabaeoidea: Cetoniidae) on woody substrates. E. Micó et al. Journal of Natural History Vol. 45, Nos. 41–42, 2011, 2527–2542











